
Reações de substituição são processos químicos em que uma substância orgânica é colocada em um mesmo meio (recipiente) que uma substância inorgânica, tendo como resultado a formação de substâncias diferentes, uma inorgânica e as outras orgânicas (dependendo da quantidade de carbonos no reagente).
Entre as substâncias orgânicas utilizadas nas reações de substituição estão alcanos, benzenos e haletos orgânicos, enquanto que as substâncias inorgânicas mais utilizadas são ácido sulfúrico (H2SO4), ácido nítrico (HNO3) e substâncias simples halogenadas (flúor-F2, cloro-Cl2, bromo-Br2 ou iodo-I2).
Veja também: substâncias simples e compostas
Existem algumas reações de substituição em que ambos reagentes são orgânicos. Nesses casos, geralmente, utiliza-se um haleto orgânico (radical ligado a um halogêneo) ou um cloreto de ácido (substância que apresenta um halogêneo ligado a uma carbonila – carbono que realiza uma ligação dupla com oxigênio) como segundo reagente.
Veja também: Tipos de reações orgânicas
O princípio básico da reação de substituição é a troca mútua de um componente entre os reagentes. Essa troca envolve as seguintes etapas:
-
1ª – Quebra da ligação existente entre halogêneos, entre nitrogênio e hidroxila (no HNO3), entre oxigênio e hidroxila (no H2SO4), entre carbono e halogêneo (no haleto orgânico), entre hidrogênio e hidroxila (no H2O).
-
2o – Quebra da ligação entre carbono e hidrogênio (no alcano ou no benzeno).
-
3o – Formação de novas ligações entre átomos ou grupos que foram inicialmente separados.
A equação abaixo exemplifica uma reação de substituição:
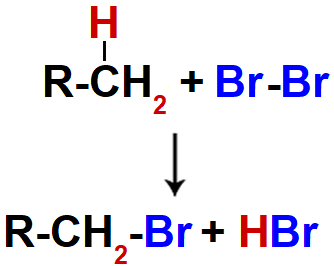
Equação química que representa uma reação de substituição
É possível observar na equação acima que há o rompimento da ligação entre o carbono e um hidrogênio, bem como da ligação entre os halogêneos. Em seguida, um halogêneo liga-se ao carbono, enquanto o hidrogênio liga-se com o outro halogêneo.
1- Reações de substituição em alcanos
1.1- Halogenação
Reação de substituição em que um alcano (R-CH3) reage com uma substância simples halogenada (Cl2), formando haleto orgânico (R-CH2-Cl) e hidrácido halogenado (HCl), ácido que apresenta hidrogênio ligado a um átomo de halogêneo). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do alcano e de um átomo de halogêneo da substância simples halogenada.
Equação representando a halogenação de um alcano qualquer
O hidrogênio interage com o átomo de halogêneo, formando um hidrácido halogenado. O outro átomo de halogêneo que restou da substância halogenada liga-se ao alcano, formando um haleto orgânico.
Obs.: Essa reação deve acontecer na presença de luz.
1.2- Nitração
Reação de substituição em que um alcano (R-CH3) reage com HNO3 (ou HO-NO2), formando nitrocomposto (R-CH2-NO2) e água (H-OH). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do alcano e de um grupo hidroxila (OH) do ácido nítrico.
Equação representando a nitração de um alcano qualquer
O hidrogênio interage com a hidroxila, formando água, enquanto o grupo nitro (NO2) restante do ácido liga-se ao alcano formando um nitrocomposto.
1.3- Sulfonação
Reação de substituição em que um alcano (R-CH3) reage com H2SO4(ou HO-SO3H), formando ácido sulfônico (R-CH2-SO3H) e água (H-OH). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do alcano e de um grupo hidroxila (OH) do ácido sulfúrico.
Equação representando a sulfonação de um alcano qualquer
O hidrogênio interage com a hidroxila, formando água, enquanto o grupo SO3H restante do ácido liga-se ao alcano formando o ácido sulfônico.
2- Reações de substituição no benzeno
2.1- Halogenação
Reação de substituição em que um benzeno (C6H6) reage com uma substância simples halogenada (Cl2), formando um haleto orgânico aromático (C6H6Cl) e um hidrácido halogenado (HCl). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do benzeno e de um átomo de halogêneo da substância simples halogenada.
Equação representando a halogenação do benzeno
O hidrogênio interage com o átomo de halogêneo, formando hidrácido halogenado, enquanto outro átomo de halogêneo restante da substância halogenada liga-se ao benzeno, formando o haleto orgânico aromático.
Obs.: Essa reação acontece na presença do catalisador cloreto de ferro III (FeCl3).
2.2- Sulfonação
Reação de substituição em que um benzeno (C6H6) reage com o ácido sulfúrico (H2SO4), formando um ácido benzenossulfônico (C6H6 SO3H) e água (H-OH). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do benzeno e de um grupo hidroxila (OH) do ácido sulfúrico.
Equação representando a sulfonação do benzeno
O hidrogênio interage com a hidroxila, formando água, enquanto o grupo SO3H restante do ácido liga-se ao benzeno, formando o ácido benzenossulfônico.
Obs.: Essa reação ocorre na presença de calor (Δ).
2.3- Nitração
Reação de substituição em que o benzeno (C6H6) reage com o ácido nítrico (HNO3), formando nitrobenzeno (C6H6 NO2) e água (H-OH). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do benzeno e de um grupo hidroxila (OH) do ácido nítrico.
Equação representando a nitração do benzeno
O hidrogênio interage com a hidroxila, formando água, enquanto o grupo NO2 restante do ácido liga-se ao benzeno, formando o nitrobenzeno.
Obs.: essa reação ocorre na presença de calor e do ácido sulfúrico, atuando como um catalisador.
2.4- Alquilação
Reação de substituição em que um benzeno (C6H6) reage com um haleto orgânico (R-Br), formando um benzeno ramificado (C6H6R) e um hidrácido halogenado (HBr). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do benzeno e de um radical do haleto orgânico (R).
Equação representando a alquilação do benzeno
O hidrogênio interage com o átomo de halogêneo, formando um hidrácido halogenado, enquanto o radical restante do haleto liga-se ao benzeno, formando um benzeno ramificado.
Obs.: Essa reação acontece na presença da substância cloreto de alumínio (AlCl3) e de aquecimento.
2.5- Acilação
Reação de substituição em que um benzeno (C6H6) reage com um cloreto de ácido (RCOCl) orgânico, formando uma cetona (C6H6COR) e um hidrácido halogenado (HCl). A formação desses produtos ocorre em decorrência da saída de um hidrogênio do benzeno e do halogêneo do cloreto.
Equação representando a acilação do benzeno
O hidrogênio interage com o átomo de halogêneo, formando um hidrácido halogenado, enquanto a carbonila restante do cloreto de ácido liga-se ao benzeno, formando uma cetona.
Obs.: Essa reação acontece na presença da substância cloreto de alumínio e de aquecimento.
3- Reações de substituição em haletos orgânicos
Reação de substituição em que um haleto orgânico (R-Br) reage com a água (H2O ou H-OH), formando um álcool (R-OH) e um hidrácido halogenado (HBr), ácido que apresenta apenas o hidrogênio e um átomo de halogêneo). A formação desses produtos ocorre em decorrência da saída do átomo de halogêneo do haleto orgânico e de um hidrogênio (H) da água.
Equação representando a substituição de um haleto orgânico qualquer
O hidrogênio interage com o halogêneo, formando o hidrácido halogenado, enquanto o grupo OH restante da água liga-se ao que restou do haleto orgânico, formando um álcool.
Obs.: Essa reação acontece na presença da substância hidróxido de sódio (NaOH) e de aquecimento.
Por Me. Diogo Lopes Dias


