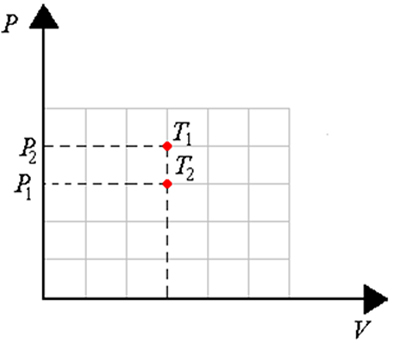
Em processos isovolumétricos, o volume permanece constante e não há, portanto, realização de trabalho. O calor trocado com o meio é igual à variação da energia interna do sistema (veja o gráfico acima).
De acordo com a Primeira lei da Termodinâmica, em qualquer processo termodinâmico a quantidade de calor Q recebida por um sistema é igual ao trabalho realizado por ele mais a variação da sua energia interna. Sendo assim, a equação que representa a primeira lei segue abaixo:
Q=τ+∆U
Como enunciado no primeiro parágrafo, onde se diz que não há realização de trabalho, temos que τ=0. Assim, o calor trocado com o meio é igual ao aumento da energia interna do sistema. Dessa forma, temos:
Q=∆U
Quando for fornecido calor para o sistema, ou seja, quando Q for positivo, a energia interna aumentará; e quando o sistema perder calor, ou seja, quando Q for negativo, a energia interna diminuirá. Os processos com volume constante ocorrem quando o recipiente que contém o material é rígido (por exemplo, um botijão de gás).
Ao receber calor, o sistema tende a expandir-se, mas é impedido pelas paredes do recipiente, portanto a pressão e a temperatura do sistema aumentam.
Por Domiciano Marques
Graduado em Física
